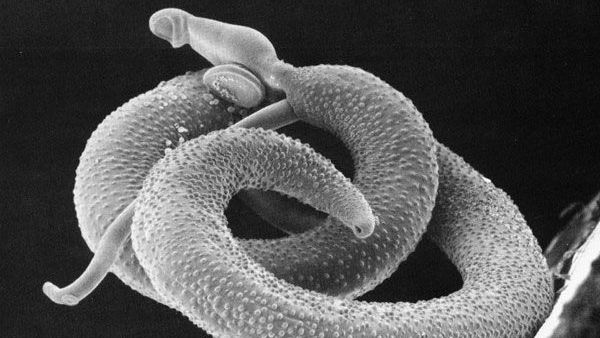
Um estudo conduzido por pesquisadores do Instituto Butantan e da USP (Universidade de São Paulo) estabeleceu um novo marco na compreensão genética do Schistosoma mansoni, o verme responsável pela esquistossomose.
Publicado na revista Non-Coding RNA, o trabalho utilizou métodos de bioinformática para identificar milhares de novos RNAs longos não codificantes (lncRNAs) no genoma do parasita. Os resultados ampliam significativamente o conhecimento sobre a biologia do organismo e abrem caminho para a identificação de novos alvos terapêuticos capazes de superar limitações dos tratamentos atuais.
Conhecida popularmente como barriga d’água, a esquistossomose é uma infecção parasitária causada por vermes do gênero Schistosoma. A transmissão ocorre em ambientes de água doce contaminada, onde larvas microscópicas liberadas por caramujos, chamadas cercárias, penetram ativamente pela pele durante o contato com a água. “Você não precisa ter uma ferida para ela entrar. Ela secreta proteases que ‘comem’ a pele e permitem a penetração”, explica o professor Sergio Verjovski-Almeida, coordenador do estudo.
Após atravessar a pele, a cercária perde a cauda e se transforma em esquistossômulo. Nesse estágio, o parasita entra na corrente sanguínea, passa pelo coração e pelos pulmões e segue até as veias do fígado. Ali, alimenta-se de sangue e amadurece até a fase adulta, diferenciando-se em macho ou fêmea. O macho, mais robusto, possui uma estrutura chamada canal ginecóforo, onde a fêmea, mais delgada, se aloja, formando um par que permanece unido por toda a vida. Juntos, migram para as veias mesentéricas, que drenam o intestino. A partir daí, a fêmea passa a produzir ovos: parte deles é eliminada nas fezes, permitindo a continuidade do ciclo, mas outra parte fica retida no hospedeiro humano e é levada pela circulação, desencadeando inflamações e lesões, especialmente no fígado.
Atualmente, o tratamento da esquistossomose depende do praziquantel, único medicamento recomendado pela OMS (Organização Mundial da Saúde). Apesar de amplamente utilizado, o fármaco apresenta limitações importantes. Ele não é eficaz contra as formas iniciais do parasita e só passa a agir após a sua maturação. Nesse estágio, as lesões no fígado já podem ter começado. Além disso, o medicamento não impede as reinfecções.
“Em áreas endêmicas, a população de parasitas é exposta a doses repetidas de praziquantel, o que pode favorecer o surgimento de resistência”, afirma Verjovski-Almeida. Já há indícios de redução na eficácia do tratamento. “Para interromper o ciclo da doença, seria fundamental identificar novos alvos terapêuticos que atuem logo após a infecção e, idealmente, até uma vacina”, acrescenta.
Com esse objetivo, os pesquisadores voltaram sua atenção para os genes não codificantes, especialmente os que dão origem aos RNAs longos não codificantes (lncRNAs). Embora não produzam proteínas, esses genes geram moléculas de RNA capazes de regular diversos processos biológicos no parasita. Diferentemente dos genes codificadores, que tendem a ser altamente conservados entre espécies, os lncRNAs apresentam grande variabilidade. Na prática, isso significa que os lncRNAs podem ser alvos mais específicos do parasita, com menor risco de afetar o hospedeiro humano, reduzindo significativamente a possibilidade de toxicidade ou efeitos colaterais no uso de fármacos baseados em silenciamento gênico.
Transcriptoma
Para construir o estudo – apoiado pela Fapesp (projetos 18/23693-5, 23/14590-6 e 21/06005-0) –, os pesquisadores reuniram quase 1.800 conjuntos de dados públicos de transcriptoma (conjunto de RNAs transcritos por uma célula, tecido ou organismo) e os integraram à versão mais atualizada e completa do genoma de Schistosoma mansoni. A equipe adotou uma abordagem de “montagem hierárquica do transcriptoma”. Em vez de analisar uma amostra mista, os cientistas processaram separadamente os dados de cada estágio do ciclo de vida do parasita: ovo, miracídio, esporocisto, cercária, forma juvenil e adultos (macho e fêmea). Segundo Verjovski-Almeida, essa estratégia permitiu detectar transcritos de baixa expressão, como os lncRNAs, que normalmente passam despercebidos em análises globais dominadas por genes mais abundantes.
Ao todo, foram identificados mais de 10 mil novos genes de lncRNA, somando quase 17 mil novos transcritos. Muitos desses RNAs apresentam marcas epigenéticas típicas de genes funcionalmente ativos, o que indica que não se trata apenas de “ruído genético”, mas de elementos regulatórios relevantes. O estudo também mostra que cerca de 42% dos lncRNAs são expressos em apenas uma fase do ciclo de vida do parasita, sugerindo funções altamente especializadas.
Machos e fêmeas
Um dos achados mais importantes do estudo está na relação entre lncRNAs e o dimorfismo sexual do parasita. Ao comparar vermes machos e fêmeas, os pesquisadores identificaram quase 2 mil genes diferencialmente expressos, incluindo 635 lncRNAs. Nos machos, esses RNAs estão associados principalmente a processos estruturais, como o desenvolvimento muscular, essencial para o acasalamento. Já nas fêmeas, regulam processos ligados à replicação de DNA e ao metabolismo, refletindo a intensa produção de ovos.
Esse resultado é particularmente relevante porque a fêmea do parasita tem uma capacidade reprodutiva extremamente alta. “A fêmea coloca 300 a 500 ovos por dia. Isso exige uma maquinaria de replicação muito grande”, explica o coordinator do estudo. Como os ovos são os principais responsáveis pelos danos ao organismo, interferir nesse processo pode ser uma estratégia eficaz de controle. “Talvez não seja necessário matar o parasita. Se ela não colocar ovos, você interrompe a transmissão e também evita a destruição do fígado”, afirma.
Os próximos passos da pesquisa envolvem validar experimentalmente esses candidatos e explorar seu potencial terapêutico. Segundo Verjovski-Almeida, a ideia é avançar para testes funcionais que confirmem o papel desses RNAs no parasita. “O próximo passo será o silenciamento desses genes in vitro e, posteriormente, in vivo”, diz. Paralelamente, o grupo segue aprimorando as análises computacionais. “Estamos aperfeiçoando as análises em larga escala com ferramentas de bioinformática para priorizar os candidatos mais promissores como alvos terapêuticos, com potencial para controlar a proliferação do parasita”, conclui.
*Thabata Oliveira é bolsista de Jornalismo Científico da FAPESP vinculada ao IQ-USP.
Verme “perdido” é redescoberto após 70 anos em cavalos-marinhos